S’il y a bien une chose qui nous tient tous réveillés la nuit, c’est cette fameuse question à savoir s’il est possible d’avoir un enfant dans l’espace… Bon d’accord peut-être pas, mais cela a tout de même piqué la curiosité de certains chercheurs.
Il faut savoir qu’il s’agit d’un sujet tabou pour la NASA, qui semble mal à l’aise à l’idée de mettre l’argent des contribuables dans ce type de projet. Bien que peu discuté, ils ont évalué de grands risques pour une astronaute en voyage tels que des fausses couches, des grossesses ectopiques ou la naissance d’un bébé prématuré. Pour assurer qu’il n’y ait pas de risques de grossesse, les femmes doivent être sur la pilule contraceptive et faire un test de grossesse avant le décollage (Proshchina et al., 2021).

D’autres compagnies privées ont poussé les recherches de leur côté. Bien sûr, pour des raisons éthiques, il n’était pas possible de tester avec des femmes enceintes. Ils ont dû se contenter d’autres animaux tels que des poissons, des amphibiens, des oiseaux et même des rats (Ronca et al., 2014 ; Proshchina et al., 2021). Ils ont observé plusieurs problématiques d’une grossesse dans l’espace, débutant du décollage jusqu’à l’accouchement. Penchons-nous vers un problème en particulier : la microgravité.
Alors qu’une pression gravitationnelle trop forte dû au décollage peut être problématique, l’absence de gravité, quant à elle, apporte aussi son lot de défis. Et cela commence par les parents eux-mêmes.
La microgravité entraîne des répercussions sur les niveaux hormonaux, autant pour les femelles que les mâles. Pour les femelles, le cycle œstral hormonal est perturbé, ce qui entraîne une diminution de production d’œstrogène, hormone nécessaire au bon développement fœtal (Ronca et al., 2014). De même pour les mâles, cette faible gravité entraîne une diminution testiculaire et donc de testostérone. Cette hormone permet le développement et la maturation des spermatozoïdes qui se retrouvent en moins grand nombre (Mishra & Luderer, 2019).
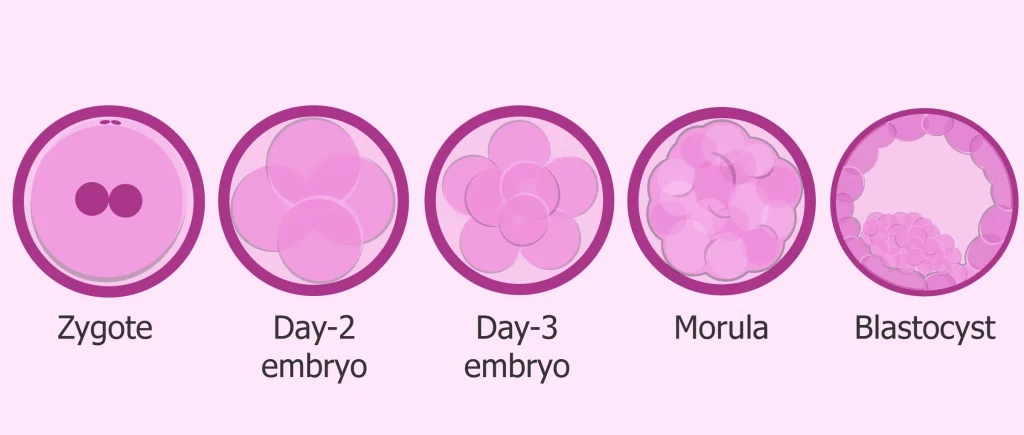
Au niveau du bébé, ce dernier est lui aussi affecté par la microgravité, et ce, depuis son développement en temps qu’embryon. Les premières semaines de développement sont particulièrement affectées par la gravité, en commençant par la division cellulaire tel qu’il a été observé chez des rongeurs. La mauvaise division cellulaire entraîne un nombre incorrect de cellules. La compaction du blastocyste n’est pas réalisée comme à l’habitude (Lei et al., 2019).
Cela entraîne des répercussions sur tout le développement des différents systèmes. Il a été observé une malformation du cerveau avec une diminution de la matière grise. Il y a un moins grand nombre de connexions neuronales, ce qui peut affecter les transmissions synaptiques (Proshchina et al., 2021). Le système cardiovasculaire est aussi impacté en l’absence de gravité. La pression artérielle est uniformisée suite à l’élimination de la pression hydrostatique, ce qui entraîne un moins grand effort pour le cœur. Habituellement plus épaisse due à une plus grande demande pour pousser le sang à travers tout le corps, la paroi ventricule gauche se voit atrophiée (Hughson et al., 2018). Il est alors à se demander si tous les tissus seront correctement oxygénés et nourris. On s’entend que les systèmes nerveux et cardiovasculaire sont primordiaux pour le développement et la survie du bébé. Cependant, le système squelettique, endocrinien, reproducteur et plusieurs autres sont aussi affectés par la microgravité (Proshchina et al., 2021; Ronca et al., 2014).
Et si, par miracle, le fœtus réussit à se développer correctement, rien n’est encore joué. En effet, le fœtus humain a besoin de la gravité pour tourner et avoir la tête vers le bas. Sans cela, l’accouchement ne peut se faire naturellement et il faut passer par césarienne. N’ayant pas l’espace pour une salle d’opération stérile dans le vaisseau, la césarienne n’est pas réaliste. Et même si le fœtus se tourne correctement, l’accouchement sera extrêmement difficile pour la mère. Les changements gravitationnels viennent affecter les neurotransmetteurs de l’ocytocine, hormone nécessaire pour les contractions utérines (Ronca et al., 2014). Entre la baisse d’ocytocine et les muscles pelviens atrophiés par l’absence de gravité, la mère devrait pousser encore plus intensément pour expulser le bébé. Ce problème a été observé chez des rats dans l’espace. La sortie du premier bébé, étant plus longue qu’à la normale, a bloqué le passage des autres bébés qui ont fini morts asphyxiés (Proshchina et al., 2021).
Tous ces problèmes et plus encore démontrent la complexité d’avoir un bébé dans l’espace. Depuis la reproduction à l’accouchement, les conditions spatiales apportent leur lot d’embuches. Qui sait, peut-être arriverons-nous à contrer ces problèmes un à la fois. Mais alors viendrait un tout nouvel enjeu : dans quelles conditions pourrait vivre ce petit être?
Bibliographie
Hughson, R. L., Helm, A., & Durante, M. (2018). Heart in space: effect of the extraterrestrial environment on the cardiovascular system. Nature reviews. Cardiology, 15(3), 167–180. https://doi.org/10.1038/nrcardio.2017.157
Lei, X., Cao, Y., Zhang, Y. et Duan, E. (2019). Advances of mammalian reproduction and embryonic developement under microgravity. Dans E. Duan et M. Long (eds.), Life Science in Space: Experiments on Board the SJ-10 Recoverable Satellite (1re éd., vol. 1, p.281-315). Science Press Bejing and Springer Nature Singapore. https://doi.org/10.1007/978-981-13-6325-2_11
Mishra, B., & Luderer, U. (2019). Reproductive hazards of space travel in women and men. Nature reviews. Endocrinology, 15(12), 713–730. https://doi.org/10.1038/s41574-019-0267-6
Proshchina, A., Gulimova, V., Kharlamova, A., Krivova, Y., Besova, N., Berdiev, R., & Saveliev, S. (2021). Reproduction and the Early Development of Vertebrates in Space: Problems, Results, Opportunities. Life (Basel, Switzerland), 11(2), 109. https://doi.org/10.3390/life11020109
Ronca, A. E., Baker, E. S., Bavendam, T. G., Beck, K. D., Miller, V. M., Tash, J. S., & Jenkins, M. (2014). Effects of sex and gender on adaptations to space: reproductive health. Journal of women’s health (2002), 23(11), 967–974. https://doi.org/10.1089/jwh.2014.4915





