Contexte
Depuis deux ans, je mène des recherches en chirurgie orthopédique à lâHôpital Shriners pour enfants – Canada sous la supervision dâun chirurgien orthopédique. Lâéquipe de recherche est principalement composée dâétudiants universitaires, ainsi que de membres du personnel hospitalier, tels des ergothérapeutes, des physiothérapeutes, des médecins et des infirmières ainsi que des statisticiens. Tout au long de lâannée universitaire, lâéquipe travaille sur plusieurs projets à la fois, avec pour objectif de pousser encore plus loin les recherches et connaissances en orthopédie pédiatrique. Nous réalisons des études prospectives et rétrospectives, visant le peaufinage des opérations chirurgicales ainsi que lâamélioration des programmes de prévention et de réhabilitation.
Présentement, nous travaillons sur un projet qui vise à évaluer les tendances en ce qui concerne lâadministration des opioïdes chez des patients pédiatriques ayant subi une chirurgie du genou (au niveau du ménisque ou du ligament croisé antérieur), dans lâespoir dâobtenir des données empiriques qui justifieraient la diminution considérable de ces drogues lors de futures opérations. Non seulement ce sujet est fascinant dâun point de vue scientifique (câest-à -dire pour lâétude des mécanismes cellulaires de la suppression de la douleur et de la toxicomanie), mais câest également une excellente occasion de se renseigner sur une épidémie dévastatrice qui prend la vie de milliers de Canadiens chaque année: la crise des opioïdes.
La crise des opioïdes affecte à ce jour des millions de patients à travers lâAmérique du Nord. Un pourcentage alarmant dâutilisateurs chroniques des opioïdes sont malheureusement devenus dépendants suite à des prescriptions légales par un professionnel de la santé. En effet, on note une augmentation marquée des prescriptions dâopioïdes depuis les 30 dernières années, passant de 76 millions en 1990 à plus 250 millions en 2015.
Les opioïdes sont une classe de médicaments analgésiques principalement utilisés en milieu hospitalier pour traiter la douleur post-opératoire et chronique. Leur efficacité à gérer et même réprimer la douleur est remarquable, or ils sont extrêmement addictifs et comportent une liste impressionnante dâeffets secondaires à court terme : nausées, vomissements, constipation, déficit sexuel chez les hommes, sensation dâeuphorie, maux de tête et étourdissements. Cependant, ce sont les effets à long terme qui sont plus inquiétants : tolérance accrue qui conduit à la dépendance et à lâabus, lésions hépatiques, infertilité chez les femmes et symptômes de sevrage potentiellement mortels.
Lâagence de la santé publique du Canada (PHAC) et les Centres pour le Contrôle et la Prévention des maladies des Ãtats-Unis (CDC) estiment quâil y a un abus des opioïdes à lâéchelle du continent, menant à une crise de santé publique qui dévaste nos familles et communautés. Pour tenter de contrer cette crise, la communauté scientifique explore de nouvelles méthodes de contrôle et de suppression de la douleur, visant surtout la diminution des effets secondaires et de la dépendance. En voici un exemple : le développement de modèles multimodaux de la douleur, qui, en gros, étudient la transduction par les nerfs périphériques du signal de la douleur depuis le site de la lésion jusquâaux centres de douleurs dans la moelle épinière et le cerveau.
Présentement, il existe très peu dâétudes dans la littérature médicale qui visent à lâamélioration de la gestion de la douleur chez les patients pédiatriques et aucune dâentre elles ne définit lâétat actuel de lâadministration dâopioïdes chez des patients pédiatriques qui ont subi une chirurgie arthroscopique du genou. Ainsi, lâéquipe de recherche de lâhôpital Shriners vise à combler ce manque. Plus précisément, nous réalisons une évaluation quantitative de lâadministration dâopioïdes avant, pendant, et immédiatement après une chirurgie arthroscopique du genou chez environ 350 patients. Dâun côté qualitatif, nous tentons de déterminer le niveau de douleur moyen chez ces patients via des scores de douleurs (FAS). Avec ces données, nous espérons mettre au clair lâétat actuel de lâutilisation de ces drogues chez cette population cible, dans le but de réduire lâadministration des opioïdes.
Survol du mécanisme biocellulaire de la suppression de la douleur
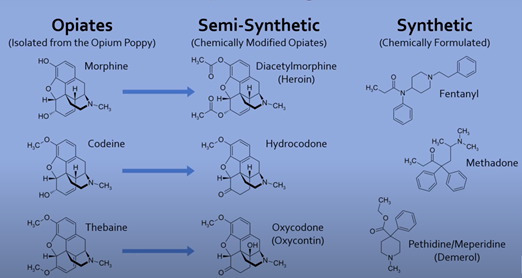
Il existe trois catégories principales dâopioïdes :
- Opiacé (isolé de la capsule du pavot) : morphine et codéine
- Semi-synthétique (modifiée chimiquement) : hydromorphone et hydrocodone, diacétylmorphine (héroïne)
- Synthétique (artificielle) : fentanyl, méthadone, mépéridine
Ces drogues imitent les molécules analgésiques produites naturellement dans notre corps en réponse à la douleur. Celles-ci comprennent les endorphines, les enképhalines et les dynorphines, qui partagent tous un motif dâacides aminés commun: Tyr-Gly-Gly-Phe.
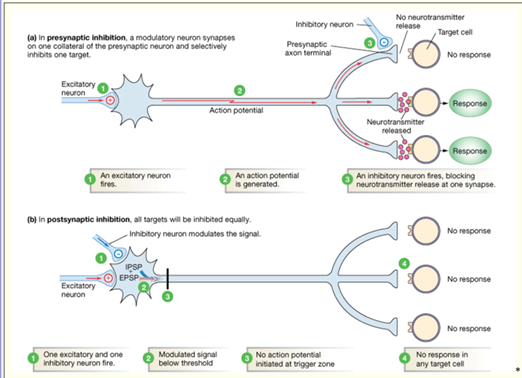
Les médicaments opioïdes et ces analgésiques endogènes fonctionnent de manière très similaire, en commençant par leur liaison à un récepteur opioïde, suivi dâune inhibition de la transduction du signal dans les neurones. On observe donc une inhibition de la voie ascendante de la douleur (responsable de la transmission des signaux de douleur des zones périphériques jusquâau système nerveux central) et lâactivation de la voie descendante de la douleur, responsable du blocage de la voie ascendante via le neurotransmetteur inhibiteur GABA, dans le but de diminuer la perception de la douleur.
Les peptides opioïdes voyagent via le système circulatoire. Pour que le médicament ait un effet, il doit atteindre le SNC en traversant la barrière hémato-encéphalique hautement sélective. Naturellement, les petits médicaments hydrophobes auront plus de facilité à pénétrer cette barrière que les gros médicaments hydrophiles. Une fois que le complexe récepteur-ligand sâest formé à la surface du neurone et que la transduction du signal sâest initiée, deux évènements se produisent, inhibant ainsi la communication neuronale :
- Lâinhibition présynaptique, qui empêche le relâchement du Glutamate (neurotransmetteur) par le neurone pré-synaptique
- Lâinhibition postsynaptique, qui empêche la dépolarisation du neurone post-synaptique
Examinons de plus près les récepteurs dâopioïde: ces derniers sont classés comme des récepteurs transmembranaires couplés à une protéine G (GPCR). Quand un opioïde se lie à son récepteur, cela provoque un changement de conformation au niveau du récepteur. La sous-unité alpha sâactive suite à sa phosphorylation et elle se dissocie des sous-unités beta et gamma.
Lors de lâinhibition présynaptique, les sous-unités beta-gamma relâchées se lient aux canaux voltage-dépendants de calcium et les bloquent. Ainsi, la propagation du potentiel dâaction, responsable de la propagation du sentiment de la douleur, est mise à lâarrêt, puisquâil nây plus dâinflux de calcium et donc pas de relâchement de neurotransmetteurs.
Lors de lâinhibition post-synaptique, les sous-unités beta-gamma relâchées se lient aux canaux potassiques (eux-mêmes liés à un GPCR) GIRK/Kir3 et les ouvrent, causant alors une violente sortie dâions potassiques intracellulaires vers le milieu extracellulaire. Ainsi, même si la vésicule présynaptique parvient à relâcher un neurotransmetteur (débutant ainsi la dépolarisation du neurone postsynaptique), la perte de charge positive due à la sortie des ions potassiques annulerait tout de même la contribution des ions de sodium entrant, ce qui entraînerait lâarrêt de la propagation du signal.
La dépendance
La dépendance envers les drogues est un phénomène extrêmement compliqué et ne peut être adéquatement exploré si lâon omet ses origines psycho-sociales. Cependant, ces domaines dépassent malheureusement mes connaissances, alors je me contenterai des explications biologiques.
Un bref aperçu de la voie de récompense du cerveau
Les neurones dopaminergiques dans lâaire tegmentaire ventrale (ATV) relâchent la dopamine et activent les noyaux accumbens, stimulant le cerveau et causant ainsi lâeuphorie.
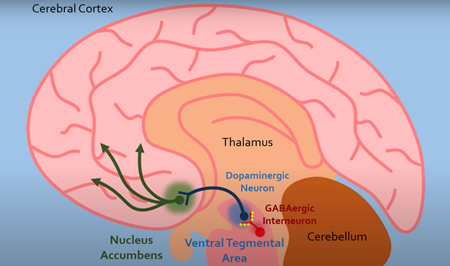
Habituellement, ces neurones dopaminergiques sont inhibés par les interneurones GABAergiques qui possèdent les récepteurs dâopioïdes. Lors de la liaison de la drogue à son récepteur, la libération de GABA est inhibée et les neurones dopaminergiques sont libres de relâcher de plus en plus de dopamine. Ainsi, après plusieurs utilisations répétées de la drogue, lâassociation entre les opioïdes et le plaisir se forme.
La tolérance et le sevrage
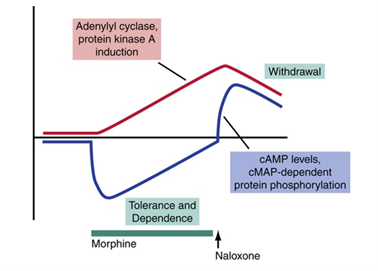
Le développement de la tolérance (ou habituation) résulte dâune absence dâinhibition de la production dâAMPc. Puisque les opioïdes diminuent les niveaux dâAMPc, les neurones en surproduisent de manière préventive afin de compenser ce manque. Ainsi, pour quâune personne puisse ressentir lâeffet désiré, elle doit prendre des doses de plus en plus fortes à chaque fois pour lutter contre la réponse physiologique du corps, qui tente de répondre au taux anormalement bas dâAMPc. De plus, plusieurs études ont démontré que la tolérance pourrait également se bâtir grâce à des mécanismes nâimpliquant pas lâAMPc, tels que des changements dans la structure du site de liaison, ainsi que lâinternalisation et le découplage des récepteurs.Pendant le sevrage, les niveaux dâAMPc neuronaux restent élevés car le mécanisme de compensation nâest plus annulé par lâutilisation des opioïdes. Les neurones deviennent donc hyperactifs, notamment dans le locus ceruleus, contribuant alors à des symptômes de sevrage mentionnés précédemment. Malheureusement, pour la plupart des gens, la seule façon dâéviter ces symptômes est de continuer à se procurer et utiliser ces drogues peu importe les conséquences.
Surdose
Une surdose dâopioïdes est mortelle, car elle provoque une dépression respiratoire. La régulation de la respiratoire sâeffectue dans le complexe de pré-Bötzinger dans le tronc cérébral. Celui-ci possède des chimiorécepteurs mesurant en permanence les niveaux sanguins dâoxygène et de dioxyde de carbone et des interneurones rythmiques qui envoient des signaux au diaphragme et aux muscles intercostaux pour maintenir la respiration.
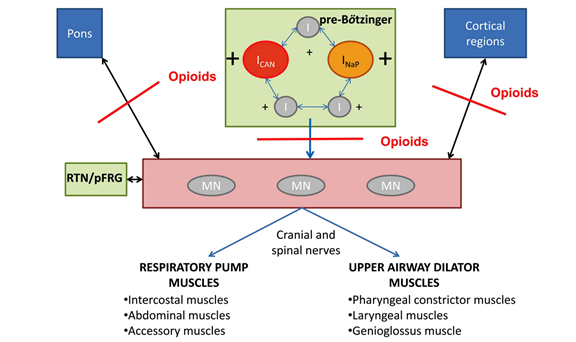
Cependant, les chimiorécepteurs et les interneurones de ce complexe possèdent également des récepteurs dâopioïdes. Alors, en cas de surdose par opioïdes, les composants du complexe de pré-Bötzinger ne répondent plus aux stimuli externes, cessent de fonctionner et lâindividu finit par mourir.
Quelques observations tirées jusquâà présent de lâétude
- La majorité des patients (92%) nâont pas demandé de renouvellement de leur prescription.
- 85% des patients ont expérimenté des niveaux de douleur acceptables avec la prise de médicaments NSAID, deux à trois jours suivant lâopération.
- Les patients ayant subi des opérations plus invasives nécessitent des doses plus puissantes en post-opératoire et à la sortie.
- Il faut améliorer la compréhension chez les patients en sâassurant dâexpliquer en détail la douleur quâils ressentiront.
- Il faut améliorer la gestion de la douleur post-opératoire en utilisant une analgésie multimodale: Tylenol, NSAID, cathéters régionaux, etc.
- Il faut développer des scores de douleurs plus détaillés et adaptés à une population pédiatrique.
- Il faut sâassurer que les médecins reçoivent une formation poussée sur lâutilisation des opioïdes, notamment sur le potentiel de dépendance.
Enfin, nous savons quâune majorité des dépendances aux opioïdes naît des prescriptions abusives, mais légales, suivant les chirurgies. Afin de réduire considérablement la quantité de ces drogues dans nos communautés, il faut absolument continuer les études, comme celle-ci, visant à comprendre le mécanisme de dépendance. Il est également nécessaire éduquer la communauté des professionnels de la santé et le public général sur les effets dévastateurs de ces substances.
Sources:
- Baker D. W. (2017). History of The Joint Commission’s Pain Standards: Lessons for Today’s Prescription Opioid Epidemic. JAMA, 317(11), 1117â1118. https://doi.org/10.1001/jama.2017.0935
- CAMH. (2012). Centre de toxicomanie et de santé mentale. Retrieved December 13, 2020, from https://www.camh.ca/-/media/files/guides-and-publications-french/dyk-rx-opioidsfr.pdf
- Hawker, G. A., Mian, S., Kendzerska, T., & French, M. (2011). Measures of adult pain: Visual Analog Scale for Pain (VAS Pain), Numeric Rating Scale for Pain (NRS Pain), McGill Pain Questionnaire (MPQ), Short-Form McGill Pain Questionnaire (SF-MPQ), Chronic Pain Grade Scale (CPGS), Short Form-36 Bodily Pain Scale (SF. Arthritis Care & Research, 63(S11). doi:10.1002/acr.20543
- Kosten, T. R., & George, T. P. (2002). The neurobiology of opioid dependence: implications for treatment. Science & practice perspectives, 1(1), 13â20. https://doi.org/10.1151/spp021113
- Nestler EJ. Historical review: molecular and cellular mechanisms of opiate and cocaine addiction. Trends in Pharmacological Sciences. 2004. (25), 210â218.